دانشمندان دانشگاه ایلینوی شیکاگو فرآیندی را شناسایی کرده اند که در آن آنزیم ها می توانند از آسیب قلبی در بیماران شیمی درمانی جلوگیری کنند. آنزیمها معمولاً در میتوکندری سلول یافت میشوند، اما وقتی سلولهای قلب تحت فشار انواع خاصی از داروهای شیمیدرمانی قرار میگیرند، آنزیمها به سمت هسته سلول حرکت میکنند، جایی که میتوانند سلولها را زنده نگه دارند. مقاله “انتقال هسته ای دهیدروژنازهای میتوکندری به عنوان یک مکانیسم حفاظتی قلبی سازگار” در ارتباطات طبیعت.
آسیب قلبی ناشی از شیمی درمانی یکی از علل اصلی مرگ و میر در میان بازماندگان سرطان است. سمیت قلبی ناشی از آنتراسایکلین با آسیب شدید میتوکندریایی ایجاد می شود، اما اطلاعات کمی در مورد مکانیسم هایی که توسط آن کاردیومیوسیت ها به طور سازگار به آسیب پاسخ می دهند، شناخته شده است. ما انتقال دهیدروژنازهای چرخه اسید تری کربوکسیلیک میتوکندری (TCA) منتخب را به هسته به عنوان یک پاسخ استرس انطباقی به سمیت قلبی آنتراسایکلین در کاردیومیوسیتهای مشتق از سلولهای بنیادی پرتوان ناشی از انسان و in vivo مشاهده کردیم.
«بیان دهیدروژنازهای میتوکندریایی هدفدار هستهای، محیط متابولیک هستهای را تغییر میدهد تا عملکرد خود را هم در شرایط in vitro و هم in vivo حفظ کند. این اثر محافظتی توسط دو مسیر موازی انجام می شود: دسترسی به کروماتین ناشی از متابولیت و سیگنال دهی AMP-kinase (AMPK). بنابراین، میزان آسیب قلبی ناشی از شیمی درمانی نشان دهنده تعادل بین آسیب میتوکندری و پاسخ محافظتی است که توسط استخر هسته ای دهیدروژنازهای میتوکندری آغاز شده است. “مطالعه ما جابجایی هسته ای دهیدروژنازهای میتوکندریایی را به عنوان یک مکانیسم تطبیقی درون زا شناسایی می کند که می تواند برای کاهش آسیب قلبی مورد استفاده قرار گیرد.”
از آنجایی که شیمی درمانی بیشتر و بیشتر موثر شده است، ما تعداد بیشتری از بیماران سرطانی را نجات می دهیم. اما بخش غم انگیز این است که بسیاری از این بازماندگان اکنون مشکلات نارسایی قلبی دارند.
ظهور قلب و عروق
این امر منجر به ظهور رشته قلب و عروق شده است. اکثر تحقیقات قبلی در این زمینه بر مکانیسم هایی متمرکز بودند که داروهای شیمی درمانی به میتوکندری سلول های قلب آسیب می رساند. این تیم تحقیقاتی علاقه مند به بررسی زاویه دیگری بود: چرا قلب برخی از بیماران از آسیب فرار می کند؟ آیا چیز خاصی در مورد سلول های آنها وجود دارد که از آنها محافظت می کند؟
ابتدا تیم کشف کرد که وقتی سلولهای قلب تحت فشار شیمیدرمانی قرار میگیرند، آنزیمهای میتوکندری به سمت هسته سلول حرکت میکنند که یک پدیده غیرعادی است. جلیس رحمان، دکترا، نویسنده ارشد، پروفسور بنجامین گلدبرگ و رئیس بخش بیوشیمی و ژنتیک مولکولی UIC توضیح داد، اما آنها نمی دانستند که آیا این حرکت علت آسیب سلول است یا ابزار محافظت از آن.
او گفت: «ما واقعاً نمیدانستیم به کدام سمت میرود.
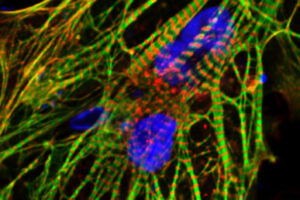
برای کشف این موضوع، محققان نسخههایی از آنزیمها را تولید کردند که به طور خاص به درون هسته حرکت کرده و میتوکندری را دور میزنند. آنها دریافتند که این جابجایی سلول ها را تقویت می کند و آنها را زنده نگه می دارد. آنها نشان دادند که این فرآیند هم در سلولهای قلب تولید شده از سلولهای بنیادی انسان و هم در موشهایی که در معرض شیمیدرمانی قرار گرفتهاند، کار میکند.
رحمان، که همچنین یکی از اعضای مرکز سرطان دانشگاه ایلینویز است، گفت: «به نظر میرسد این مکانیسم جدیدی است که سلولهای قلب میتوانند از طریق آن در برابر آسیب شیمیدرمانی از خود دفاع کنند.
این کشف احتمالات بالینی جدیدی را نشان می دهد. پزشکان میتوانند تک تک بیماران را آزمایش کنند تا ببینند آیا سلولهای قلب تولید شده از سلولهای بنیادی شخصیسازی شده، با انتقال آنزیمهایشان از میتوکندری به هسته سلول، به اندازه کافی از خود در برابر شیمیدرمانی محافظت میکنند. پزشکان میتوانند از بیمار خون بگیرند، از سلولهای خونی سلولهای بنیادی بسازند و سپس از آن سلولهای بنیادی شخصیسازی شده برای تولید سلولهای قلبی با ساختار ژنتیکی مشابه سلولهای قلب بیمار استفاده کنند.
به گفته رحمان، “ارزیابی آسیب ناشی از شیمی درمانی و حرکت آنزیم از میتوکندری به هسته سلول های قلب در آزمایشگاه به تعیین پاسخ احتمالی بیمار به شیمی درمانی کمک می کند.”
در بیمارانی که محافظت ناکافی دارند، می توان با افزایش حرکت آنزیم و محافظت از سلول های قلب، محافظت را افزایش داد.
برنامه ای برای انجام مطالعات بیشتر در مورد اینکه آیا این روش می تواند به جلوگیری از آسیب قلبی ناشی از بیماری های دیگر مانند فشار خون بالا و حملات قلبی کمک کند و اینکه آیا این روش در سلول های دیگر مانند سلول های رگ های خونی کار می کند یا خیر.