هنگامی که سلولها DNA را برای تولید رونوشتهای RNA کپی میکنند، بخشهایی از ماده ژنتیکی شامل میشود – اینها به عنوان اگزون شناخته میشوند – اما بقیه به بیرون پرتاب میشوند. رونوشت حاصل یک مولکول RNA کاملا بالغ است که می تواند به عنوان الگویی برای ساخت پروتئین استفاده شود. یکی از ویژگیهای بیان ژن این است که از طریق فرآیندی به نام پیرایش جایگزین، سلول میتواند ترکیبهای مختلفی از اگزونها را برای ساخت رونوشتهای مختلف RNA انتخاب کند. محققان به سرپرستی تیمی در مرکز تنظیم مقررات ژنومی (CRG)، مؤسسه علم و فناوری بارسلونا، مجموعهای از قطعات ژنی ریز کدکننده پروتئین معروف به میکرواکسونها را کشف کردهاند که به mRNA سلول جزایر پانکراس متصل میشوند و به نظر میرسد که نقش دارند. نقش مهمی در عملکرد جزایر و کنترل قند خون دارد و ممکن است به مستعد دیابت نوع 2 (T2D) کمک کند.
این تیم به سرپرستی پروفسور تحقیقاتی ICREA، Manuel Irimia، PhD، یک پروتئین متصل به RNA به نام SRRM3 را شناسایی کردند که این IsletMICs را تنظیم می کند و دریافتند که SRRM3 و IsletMICs هر دو با افزایش سطح گلوکز القا می شوند. سپس مطالعات آنها نشان داد که یا کاهش SRRM3 در رده های سلولی بتا انسان و موش صحرایی و جزایر موش، یا سرکوب IsletMIC های خاص، بر ترشح انسولین تأثیر می گذارد. گزارش یافته های خود در متابولیسم طبیعتمحققان کشف کردند که انواع ژنتیکی انسانی که بر بیان SRRM3 و گنجاندن IsletMIC در جزایر تأثیر میگذارند با تغییرات قند ناشتا و خطر T2D مرتبط هستند. این تیم پیشنهاد میکند که این میکرواکسونهای جزایر ممکن است اهداف امیدوارکنندهای را برای درمان سلولهای بتای ناکارآمد در T2D نشان دهند. نتایج آنها همچنین از این تصور حمایت می کند که سلول های جزایر پانکراس با قرض گرفتن مکانیسم های تنظیمی از سلول های عصبی تکامل یافته اند.
در مقاله منتشر شده با عنوان «میکرواکسون های پانکراس عملکرد جزایر و هموستاز گلوکز را تنظیم می کنند»، نویسندگان بیان کردند: «در اینجا، ما دریافتیم که زیرمجموعه ای از میکرواکسون های عصبی در جزایر پانکراس نیز وجود دارد و یک برنامه حفظ شده از نظر تکاملی را تشکیل می دهد که به ویژه بر ژن های درگیر در آن تأثیر می گذارد. عملکرد ترشحی انسولین و خطر T2D … بنابراین نتایج ما یک برنامه تنظیمی پس از رونویسی را آشکار می کند که برای عملکرد سلول های جزایر بالغ و کنترل قند خون ضروری است.
موجودات زنده از اتصال جایگزین برای فعال کردن عملکردهای پیچیده استفاده می کنند. شبیه به تولیدکنندگان فیلم که برش منظم و کارگردانی از یک فیلم را ایجاد می کنند، شامل یا حذف یک اگزون منفرد در رونوشت می تواند منجر به تولید پروتئین هایی با عملکردهای متفاوت شود. بنابراین انواع مختلف سلول ها در انواع مختلف بافت ها رونوشت های RNA متفاوتی را از یک ژن تولید می کنند. همانطور که نویسندگان توضیح دادند، «پیشگیری جایگزین، پردازش تفاضلی اینترونها و اگزونها را برای تولید ایزوفرمهای mRNA متعدد از یک رونوشت اولیه واحد تنظیم میکند و به تنوع رونوشت و پروتئومی کمک میکند. تخمین زده میشود که بیش از 95 درصد از ژنهای چند اگزونیک انسانی تحت پیرایش جایگزین قرار میگیرند، بخش قابلتوجهی از آن به شیوهای غنیشده از نوع بافت و نوع سلول تنظیم میشود.
درک نحوه عملکرد این فرآیند سرنخ های جدیدی در مورد رشد، سلامت و بیماری انسان ارائه می دهد و راه را برای اهداف تشخیصی و درمانی جدید هموار می کند. تیم تحقیقاتی ادامه داد: «مطالعات فراوانی شواهد تجربی ارائه کردهاند مبنی بر اینکه تنظیم جایگزینی پیرایش برای بسیاری از فرآیندهای بیولوژیکی ضروری است و نقش چندین پروتئین تنظیمکننده پیوند دهنده پیوند RNA را در توسعه و عملکردهای بافتی مشخص کردهاند.
میکرواکسون ها نوع جدیدی از توالی DNA کد کننده پروتئین هستند که اخیراً کشف شده است. میکرواکسونها با طول تنها سه تا ۲۷ نوکلئوتید، بسیار کوتاهتر از اگزونهای متوسط هستند، که معمولاً میانگین آن حدود ۱۵۰ نوکلئوتید است. وجود میکرواکسونها در بسیاری از گونههای مختلف از مگس گرفته تا پستانداران نشان میدهد که آنها عملکرد مهمی دارند زیرا برای صدها میلیون سال توسط انتخاب طبیعی حفظ شدهاند.
در انسان، بیشتر میکرواکسونها منحصراً در سلولهای عصبی یافت میشوند، جایی که قطعات ریز ژن نقش کلیدی دارند. به عنوان مثال، مطالعات اخیر نشان می دهد که آنها برای توسعه گیرنده های نوری، یک نوع تخصصی از نورون در شبکیه، حیاتی هستند. تحقیقات همچنین نشان داده است که تغییرات در فعالیت میکرواکسون در مغزهای اوتیستیک رایج است و نشان میدهد که این قطعات ژنی نقش مهمی در ویژگیهای بالینی این بیماری دارند.
با این حال، همانطور که تیم در مقاله جدید منتشر شده خود اشاره کرد، در حالی که پیرایش جایگزین نقش مهمی در توسعه و عملکرد انواع سلول ها و بافت ها ایفا می کند، “تأثیر آن بر غدد درون ریز پانکراس و ارتباط فیزیولوژیکی آن در زمینه کنترل قند خون تا حد زیادی ناشناخته باقی مانده است.
Irimia، یک محقق CRG که نقش عملکردی میکرواکسون ها را بررسی می کند، توضیح داد: «یک میکرواکسون قطعه کوتاهی از DNA است که برای چند اسید آمینه، بلوک های سازنده پروتئین ها، کد می کند. اگرچه ما مکانیسمهای دقیق عمل را نمیدانیم، از جمله یا حذف فقط تعداد انگشت شماری از این اسیدهای آمینه در حین اتصال، سطوح پروتئینها را به روشی بسیار دقیق تراشیده میکند. بنابراین، پیوند میکرواکسون را می توان به عنوان راهی برای انجام میکروجراحی پروتئین ها در سیستم عصبی، اصلاح نحوه تعامل آنها با مولکول های دیگر در سیناپس های بسیار تخصصی نورون ها در نظر گرفت.
مطالعات انجام شده توسط Irimia و پروفسور ICREA، Juan Valcárcel، PhD، در CRG نشان داد که میکرواکسون ها در سلول های جزایر پانکراس نیز وجود دارند، نوع دیگری از سلول ها که عملکردهای بسیار تخصصی را در بافت و اندام پیچیده انجام می دهند. کار آنها نشان داد که پیرایش میکرواکسون در جزایر پانکراس حاوی سلولهای بتا که انسولین را میسازند، شایع است.
محققان در حین مطالعه نقش جایگزینی جایگزین در بیولوژی جزایر پانکراس و حفظ سطح قند خون به کشف خود دست یافتند. آنها دادههای توالی RNA را از بافتهای مختلف انسان و جوندگان مطالعه میکردند، بهویژه به دنبال اگزونهایی بودند که در جزایر پانکراس در مقایسه با سایر بافتها به طور متفاوتی به هم متصل شدهاند.
دادههای آنها نشان داد که نیمی از اگزونهایی که به طور خاص در جزایر پانکراس غنی شدهاند، میکرواکسونها هستند که تقریباً همه آنها در سلولهای عصبی نیز یافت میشوند. آنها نوشتند: «ما دریافتیم که زیرمجموعهای از میکرواکسونهای عصبی در جزایر پانکراس نیز وجود دارد و یک برنامه حفظشده تکاملی را تشکیل میدهد که بهویژه بر ژنهای دخیل در عملکرد ترشح انسولین و خطر T2D تأثیر میگذارد». یافتهها با این ایده مطابقت دارد که سلولهای جزایر پانکراس مکانیسمهای تنظیمی را از سلولهای عصبی انتخاب کردهاند.
مطالعات این تیم نشان داد که از بیش از 100 میکرواکسون جزایر پانکراس شناسایی شده، اکثریت آنها بر روی ژن های حیاتی برای ترشح انسولین قرار دارند یا با خطر دیابت نوع 2 مرتبط هستند. این تحقیق همچنین نشان داد که گنجاندن میکرواکسون در رونوشتهای RNA توسط SRRM3، پروتئینی که به مولکولهای RNA متصل میشود و توسط ژن SRRM3 کدگذاری میشود، کنترل میشود. آزمایشها نشان داد که سطوح بالای قند خون هم بیان SRRM3 و هم شامل میکرواکسونها را القا میکند و به این احتمال اشاره میکند که تنظیم اتصال میکرواکسون میتواند در حفظ سطح قند خون نقش داشته باشد.
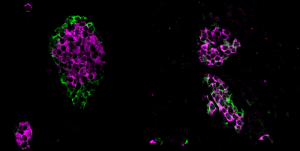
برای درک بیشتر تأثیر میکرواکسونهای جزایر، محققان آزمایشهای عملکردی را با استفاده از سلولهای بتا انسانی رشد یافته در آزمایشگاه و همچنین آزمایشهای in vivo و ex vivo با موشهای فاقد ژن SRRM3 انجام دادند. آنها دریافتند که کاهش SRRM3 یا سرکوب تک میکرواکسون ها منجر به اختلال در ترشح انسولین در سلول های بتا می شود. در موشها، تغییرات در اتصال میکرواکسون شکل جزایر پانکراس را تغییر داد و در نهایت بر ترشح انسولین تأثیر گذاشت. “به طور مداوم، تنظیم نادرست میکرواکسون ها در رده های سلولی بتا، چه در سطح جهانی از طریق کاهش SRRM3 یا به طور جداگانه با استفاده از الیگونوکلئوتیدهای آنتی سنس (ASOs)، منجر به ترشح انسولین نامنظم می شود. در همین راستا، موشهای ناک اوت Srrm3 تغییراتی در هویت سلولی جزایر، افزایش ترشح انسولین و هیپوگلیسمی پایدار نشان دادند.
محققان با گروه تحقیقاتی Jorge Ferrer، PhD، همچنین در CRG، برای مطالعه دادههای رونوشت ژنتیکی و RNA از افراد دیابتی و غیر دیابتی و بررسی ارتباطهای احتمالی بین میکرواکسونها و اختلالات متابولیک انسانی همکاری کردند. آنها دریافتند که انواع ژنتیکی که بر گنجاندن میکرواکسون تأثیر میگذارند، با تغییرات در سطح قند خون ناشتا و همچنین خطر T2D مرتبط هستند. آنها همچنین دریافتند که بیماران دیابتی نوع 2 سطوح پایین تری از میکرواکسون ها در جزایر پانکراس خود دارند. این تیم خاطرنشان کرد: «بهطور مهمی، انواع ژنتیکی انسانی که بر بیان SRRM3 و گنجاندن IsletMIC در جزایر تأثیر میگذارند، با تغییرات گلوکز ناشتا و خطر دیابت نوع 2 مرتبط هستند». ما همچنین مشاهده کردیم که IsletMICs به طور گسترده در جزایر افراد مبتلا به T2D کاهش می یابد، اثری که اخیراً در مدل موش دیابتی نیز گزارش شده است… در مجموع، این داده ها نشان می دهد که تغییرات در فعالیت SRRM3 و اهداف میکرواکسون آن بر عملکرد جزایر و هموستاز گلوکز تأثیر می گذارد. ، به طور بالقوه به استعداد T2D کمک می کند.
یافتههای این مطالعه راه را برای کشف استراتژیهای درمانی جدید برای درمان دیابت با تعدیل اتصال هموار میکند. دکتر Jonas Juan Mateu، محقق فوق دکترای CRC، که اولین نویسنده این مطالعه است، توضیح داد: «در اینجا ما نشان میدهیم که میکرواکسونهای جزایر نقش مهمی در عملکرد جزایر و هموستاز گلوکز دارند و به طور بالقوه در ابتلا به دیابت نوع 2 نقش دارند. به همین دلیل، میکرواکسون ها ممکن است اهداف درمانی ایده آلی را برای درمان سلول های بتا ناکارآمد در دیابت نوع 2 نشان دهند. ماتئو خاطرنشان کرد: طیف گسترده ای از تعدیل کننده های اتصال برای درمان انواع بیماری های انسانی در دسترس هستند. هنگامی که هشت سال پیش برای اولین بار مطالعه پیوند در جزایر پانکراس را شروع کردم، میخواستم بدانم آیا تعدیلکنندههای پیوند موجود میتوانند برای دیابت استفاده مجدد شوند یا خیر. فکر میکنم یک قدم به آن نزدیکتر شدهایم.»
در حالی که این کار نشان می دهد که میکرواکسون ها بازیگران مهمی در زیست شناسی جزایر پانکراس هستند، تحقیقات بیشتری برای تعیین تأثیر دقیق آنها در طول توسعه بافت مورد نیاز است. محققان همچنین فاقد بینش مکانیکی در مورد اینکه چگونه هر میکرواکسون منفرد عملکرد پروتئین را تغییر میدهد و مسیرهای کلیدی در سلولهای جزایر را تحت تأثیر قرار میدهد، ندارند. درک این موضوع نقش فیزیولوژیکی دقیق آنها را در دیابت و سایر بیماری های متابولیک مرتبط با جزایر پانکراس روشن می کند.
این مطالعه به شواهد فزاینده ای اضافه می کند که میکرواکسون ها نقش مهمی در رشد، سلامت و بیماری انسان دارند. کمتر از 10 سال پس از اولین گزارش وجود آنها، می بینیم که چگونه میکرواکسون ها عناصر کلیدی هستند که نحوه تعامل پروتئین ها با یکدیگر را در سلول ها با عملکردهایی که به درجه بالایی از تخصص نیاز دارند، مانند آزادسازی انتقال دهنده های عصبی یا انسولین و انتقال نور، تغییر می دهند. ایریمیا توضیح داد. در نتیجه، ما انتظار داریم که جهش در میکرواکسونها منجر به بیماریهایی شود که هنوز دلایل ژنتیکی آنها را درک نکردهایم. ما شروع به جستجوی این جهشها در بیماران مبتلا به اختلالات عصبی و متابولیکی و همچنین رتینوپاتیها کردهایم تا پس از آن مداخلات احتمالی برای درمان آنها ابداع کنیم.
همانطور که نویسندگان بیشتر نتیجه گرفتند، “در حال حاضر طیف گسترده ای از استراتژی ها برای دستکاری درمانی پیوند RNA وجود دارد. بنابراین، تحقیقات آینده در مورد عملکرد مولکولی IsletMICs و سایر اگزون های غنی شده با جزایر و نقش آنها در اختلال عملکرد جزایر ممکن است دانش ارزشمندی را نه تنها برای زیست شناسی جزایر، بلکه برای توسعه درمان های جدید برای T2D بر اساس مدولاسیون اتصال ارائه دهد.